Durchbruch bei personalisierter Krebstherapie mit Gentherapie: Der medizinische Quantensprung im Kampf gegen Krebs
Was ist der Hoffnungsträger im Kampf gegen Krebs? Wie kann ein Therapieansatz, der auf die individuellen genetischen Eigenschaften eines Tumors eingeht, das Überleben der Patienten revolutionieren? Mit genau diesen Fragen beschäftigen sich im Jahr 2025 zahlreiche Forscher, Kliniker und Start-ups, darunter auch innovative Biotech-Firmen wie BioNTech oder Moderna, die bereits in der Pandemie für Aufsehen sorgten. Aktuelle Studien und Auszeichnungen, etwa der Deutsche Krebspreis 2025, markieren eine echte Zäsur: Gentherapien und personalisierte Strategien versprechen erstmals Heilungschancen bei bislang therapieresistenten Tumoren.
Individuell statt Standard: Die personalisierte Krebstherapie im Überblick
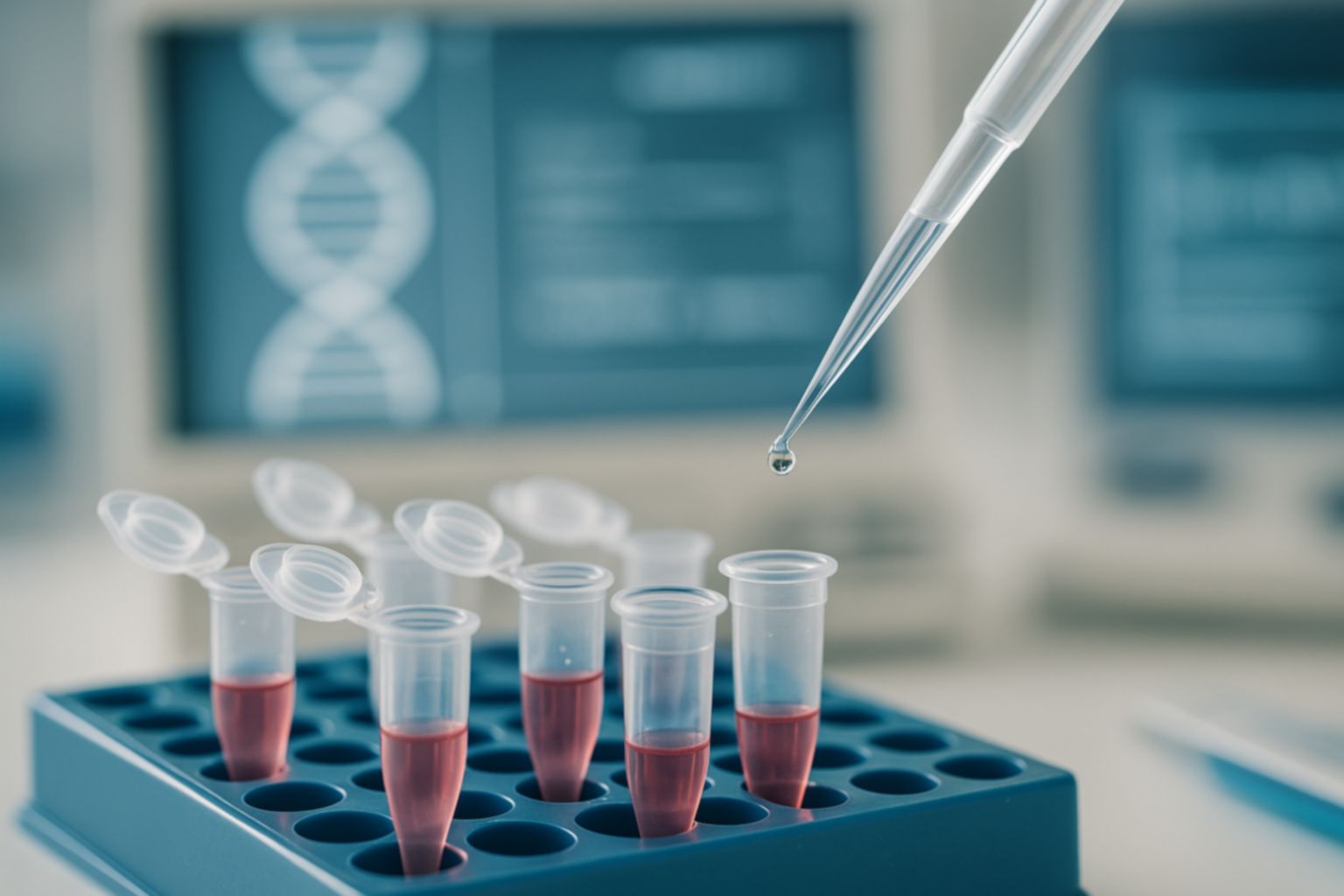
Die personalisierte Krebstherapie verfolgt einen radikal neuen Ansatz: Jeder Tumor wird als einzigartig betrachtet. Mithilfe modernster genetischer Diagnostik analysieren Forscher die spezifischen Mutationen und molekularen Eigenschaften des Tumorgewebes. Darauf aufbauend kann die Therapie exakt auf den Patienten zugeschnitten werden. Besonders innovativ sind dabei:
- mRNA-basierte Impfstoffe: Sie trainieren das Immunsystem, zielgerichtet gegen charakteristische Tumormerkmale vorzugehen. Laut aktuellen Studien an Melanompatienten liefern sie erstmals personalisierte Immunantworten mit verbesserten Überlebensraten und geringeren Nebenwirkungen. Die Ergebnisse einer Phase-3-Studie – in der Wirksamkeit und Sicherheit an großen Patientenkohorten geprüft werden – werden bereits 2026 erwartet.
- Gentherapie-Tools wie CRISPR/Cas9: Mit der Genschere lassen sich gezielt krankhafte DNA-Sequenzen ausschalten oder reparieren, was insbesondere bei erblich bedingten Krebserkrankungen, aber auch zunehmend bei sporadischen Tumoren erforscht wird.
- Tumorinfiltrierende Lymphozyten (TILs) & bispezifische Antikörper: Diese Strategien zeigen sich vor allem bei resistenten Tumoren, etwa schwarzem Hautkrebs, als zukunftsweisend. TILs können Tumore auch dann angreifen, wenn klassische Therapien versagen.
Technologischer Fortschritt: Von Patient-derived Organoids bis zu molekularen Tumorboards
Die technische Entwicklung ist maßgeblich für den jüngsten Durchbruch. Professorin Melanie Börries, Preisträgerin des Deutschen Krebspreises 2025, nutzt etwa sogenannte Patient-derived Organoids (PDOs): Mini-Organe aus Tumorbiopsien, mit denen das individuelle Ansprechen neuer Therapien getestet wird. Das bedeutet, dass Vorhersagen über Therapieerfolg und Überlebenschancen heute wesentlich präziser möglich sind als je zuvor. Zudem kommen molekulare Tumorboards zum Einsatz, in denen interdisziplinäre Experten anhand komplexer Sequenzierungsdaten maßgeschneiderte Therapieempfehlungen ausarbeiten.
Aktuelle Herausforderungen: Kosten, Zugang und Evidenzlage
Trotz großer Fortschritte bleibt die breite klinische Anwendung eine der größten Herausforderungen. Die Herstellung personalisierter Therapien ist kostenintensiv und die Prozesse, etwa bei TILs oder speziellen Antikörpern, sind bislang mit langen stationären Aufenthalten verbunden. Zudem ist die Zulassung neuer Medikamente durch komplexe Regularien verlangsamt. Es besteht die Gefahr, dass innovative Therapien zunächst nur für eine kleine Patientengruppe im Rahmen von Studien zugänglich sind.
Beispiele und Erfolge aus der Praxis
Jüngste klinische Studien mit mRNA-Impfstoffen gegen Melanome zeigen, dass Patienten von individuell zugeschnittenen Therapien profitieren: Überlebensraten steigen, Nebenwirkungen sind geringer, die Lebensqualität verbessert sich deutlich. Auch bei seltenen Tumorarten wie Aderhautmelanomen gibt es bereits zugelassene bispezifische Antikörper. Darüber hinaus werden Gentherapien für einige erbliche Erkrankungen und Leukämien als einmalige „Kur“ getestet oder eingesetzt, wobei erste Langzeiterfolge beobachtet werden.
Diskussion und Ausblick
Welche Vor- und Nachteile bringt dieser medizinische Fortschritt?
- Vorteile:
- Gezielte, effektive Therapien: Krebsbehandlungen werden wirksamer und verträglicher, insbesondere bei schwer zu therapierenden oder seltenen Tumorarten.
- Langfristige Heilungschancen: Einmalige Gentherapien bieten das Potenzial einer dauerhaften Heilung, vor allem bei bestimmten genetischen Krebsformen.
- Gestiegene Lebensqualität: Personalisiertes Vorgehen reduziert Nebenwirkungen und Krankenhausaufenthalte.
- Nachteile:
- Zugangsbeschränkungen: Durch die hohen Kosten sind neue Therapien bislang meist nur in spezialisierten Zentren verfügbar.
- Komplexe Zulassungsprozesse: Die langwierige Prüfung verzögert die breite Anwendung und erschwert die Finanzierung durch Krankenkassen.
Zukünftig ist mit schnelleren Entwicklungszyklen, sinkenden Herstellungskosten und damit besseren Zugangsmöglichkeiten zu rechnen. Der Einsatz künstlicher Intelligenz, maschinellen Lernens und bioinformatischer Tools wird die Therapieauswahl weiter verbessern. Unternehmen wie BioNTech und deren Partner treiben diesen Wandel entscheidend voran. Für die Wirtschaft ergeben sich enorme Potenziale: Die Nachfrage nach hochwertigen Biotech-Lösungen wächst, und das Gesundheitssystem steht vor einer neuen Ära personalisierter Medizin. Menschlich bedeutet das: Die Hoffnung auf echte Heilung und ein längeres, gesünderes Leben rückt für viele Krebspatienten erstmals realistisch in den Bereich des Möglichen.
Aktuelle zusätzliche Ressourcen und wirtschaftliche Ausblicke finden sich unter anderem bei den „Nachrichten des Tages beim Deutschlandfunk“ und ergänzend in den Videonachrichten von Euronews, die regelmäßig neue Marktdaten und technologische Trends beleuchten.























Kommentar abschicken